Czy szczepionka DNA będzie alternatywą dla dotychczasowych metod walki z rakiem? Obiecujące wyniki uzyskano dzięki pałeczkom Salmonelli.
Trwają badania nad opracowaniem metody leczenia nowotworu za pomocą immunoterapii (pobudzenia systemu odpornościowego do walki). Jest to dość obiecująca alternatywa dla chemii oraz naświetlań, które niszczą komórki nowotworowe, lecz powodując przy tym wiele niekorzystnych efektów ubocznych. Sądzi się, że immunoterapia będzie bezpieczniejsza i bardziej komfortowa dla pacjentów. Do tej pory przynosiła ona ograniczone rezultaty, z uwagi na to, jak trudno przyswajalne są doustne szczepionki DNA. Receptę na ten problem odnalazł być może zespół badaczy, prowadzony był przez Yuana Pinga (Nanyang Technological University w Singapurze) oraz Gupinga Tanga (Zhejiang University w Hangzhou).
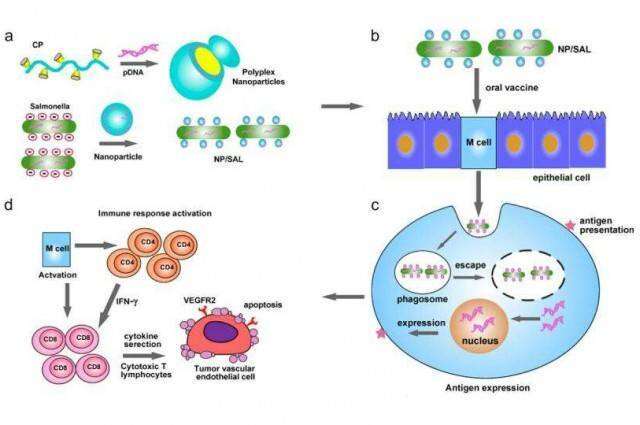
Działanie samej szczepionki (NP/SAL) polega na odcięciu zmiany patologicznej od zasobów, których guz potrzebuje do gwałtownego wzrostu. Miejscowo powstrzymuje ona proces angiogenezy, czyli powstawanie naczyń włosowatych. Są to drobne naczynia krwionośne lub limfatyczne, bezpośrednio oplatające tkanki i doprowadzające składniki odżywcze do komórek. W dostarczaniu substancji (pinocytoza) czynnie uczestniczy cieniutka ściana śródbłonka. Nowotwory produkują białka (VEGF, odpowiedzialne między innymi za przerzuty raka), które powodują jej przyrost – tu wkracza NP/SAL i niszczy śródbłonek przez stymulację układu odpornościowego do produkcji odpowiednich limfocytów typu T (białe krwinki) oraz cytokin (białka odpowiadające za reakcję immunologiczną). Teraz pozostaje kwestia – jak sprawić, by szczepionka znalazła się w odpowiedniej ilości i w odpowiednim miejscu?
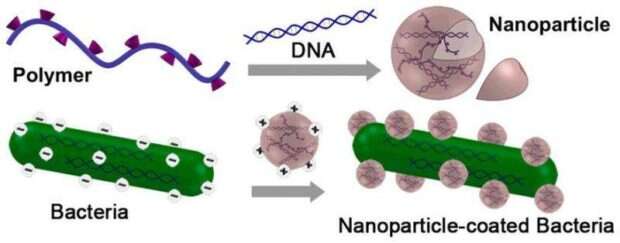
Naukowcy opublikowali wyniki badań, z których wynika, że NP/SAL może być efektywnie rozprowadzona za pośrednictwem zmodyfikowanych bakterii. Do sporządzenia tabletki użyto pałeczek Salmonelli, które najpierw osłabiono, by powodowały możliwie najmniejsze zatrucie. Następnie obleczono je w polimery dla uzyskania większej odporności na kwaśne środowisko żołądka oraz fagocyty – dodatnio naładowane nanocząsteczki polimerowe „przyklejono” do ujemnie naładowanych bakterii. Lek testowano na myszach – u 60% z nich zaobserwowano zastój rozwoju raka podczas 35 dni próby i brak skutków ubocznych. Yuan Ping określił tę metodę szczepienia jako bardzo elastyczną, prawdopodobnie możliwą do zastosowania także przy leczeniu szerokiego wachlarza chorób immunologicznych.
Źródło: Iflscience.com; Zdjęcia: American Chemical Society